L'ibridazione (o ibridizzazione) del carbonio è un argomento della chimica inorganica che funge da chiave di lettura nella comprensione della chimica organica e dei suoi composti. Alcani, alcheni, alchini… argomento facile direte voi! Beh, vi assicuro che c’è di più dietro quei legami semplici, doppi e tripli. Comprendere l'ibridazione è fondamentale per capire la geometria molecolare, la forza dei legami e la reattività dei composti organici.
Il carbonio, elemento del quarto gruppo e del secondo periodo, possiede 6 protoni e 6 elettroni. La sua configurazione elettronica allo stato fondamentale è: 1s² 2s² 2p². Questo significa che solamente due dei suoi elettroni risultano spaiati nei sottolivelli 2p (2px¹ e 2py¹). In questo modo, però, la struttura dei composti del carbonio non è giustificata. Essi infatti non costituiscono 2 legami, bensì 4! Nel metano (CH₄) ad esempio il carbonio lega 4 idrogeni, com’è possibile? La prima alternativa da considerare è L’ECCITAZIONE. Essa viene introdotta quando si ha un numero di legami dell’atomo centrale diverso dal numero di elettroni spaiati. Eccitando il carbonio gli si fornisce energia ed uno dei due elettroni presenti nell’orbitale 2s va ad occupare l’orbitale 2pz formando lo stato di tetravalenza. Anche questa disposizione elettronica però non descrive in maniera accurata la molecola di metano. Si formerebbero infatti, tre legami identici (dati dalla sovrapposizione degli orbitali p del carbonio con i tre orbitali s dell’H) e un legame diverso (dato dalla sovrapposizione di due orbitali s). Per spiegare la struttura tetraedrica del metano è necessario ricorrere all’IBRIDAZIONE. Essa viene introdotta per spiegare una geometria molecolare diversa da quella che ci si aspetterebbe con l’uso degli orbitali atomici puri.
Gli orbitali sono ibridi quando risultano dalla combinazione di orbitali diversi (es. s e p). Perché si formano gli orbitali ibridi? Per diminuire la repulsione tra gli elettroni, per formare legami più forti, perché si possano formare più legami e perché sono meglio orientati.
Il carbonio adotta tre configurazioni differenti da quelle dello stato fondamentale in base alle diverse combinazioni degli orbitali del secondo livello:
Ibridazione sp³: Il Legame Singolo Carbonio-Carbonio
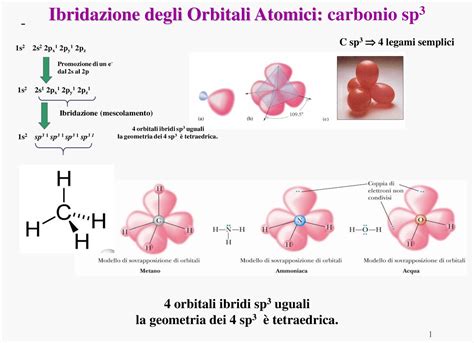
L'ibridazione sp³ si ottiene dal rimescolamento dell'orbitale s con 3 orbitali p. Si formano 4 orbitali ibridi isoenergetici. I 4 orbitali ibridi si dispongono ai vertici di un tetraedro, con angoli di 109.5°. I legami che formano con gli altri elementi sono di tipo σ, perciò molto forti. Questo tipo di ibridazione è tipico degli alcani, dove tutti i legami carbonio-carbonio sono semplici.
È il caso del metano (CH₄) e anche dell’acqua (H₂O). Entrambe le molecole si formano attraverso questo tipo di ibridazione o ibridizzazione. Per la precisione, nella molecola di metano è il carbonio (C) che si ibrida, nella molecola d’acqua è l’ossigeno (O). In questo tipo di ibridazione, l’orbitale 2s (orbitale s a livello energetico 2) di un dato elemento chimico (C o O) si fonde con i 3 sotto-orbitali dell’orbitale 2p formando 4 nuovi orbitali tutti identici tra di loro che si chiamano sp³. Si guardi la figura sottostante, in cui è spiegata la normale configurazione elettronica del carbonio (C) per capire come sono costituiti i suoi orbitali al livello energetico = 2. Come appena spiegato, quando avviene l’ibridazione orbitalica un elettrone di s migra nel sotto-orbitale vuoto di p.
PRECISAZIONE: nella molecola di metano (CH₄), gli angoli del tetraedro formato dall’orbitale s e p del livello energetico 2 del carbonio (C) sono esattamente di 109,5°. Tuttavia, nella molecola di acqua (H₂O), l’angolo formato dagli orbitali ibridati dell’ossigeno (O) è 104° circa. Dal momento che l’ossigeno, come il carbonio di CH₄, opera l’ibridazione sp³, si ritrova anch’esso con 4 elettroni spaiati, e quindi con la possibilità di formare 4 legami covalenti con l’idrogeno. Ma poi forma solo 2 legami con 2 idrogeni!
Nel metano, la loro energia di legame è di 438 kJ/mol e la loro lunghezza arriva fino a 1,10 Å. Questi sono valori caratteristici fissati per un particolare legame in quella molecola. Un’altra caratteristica della geometria di quella molecola è l’angolo di legame. Determina l’angolo formato tra due legami HCH consecutivi ed è uguale esattamente a 109,5 °. Un altro composto che può essere considerato allo stesso modo è l’etano, che contiene un legame tra atomi di carbonio (CC). Gli atomi di carbonio esistenti nella sua struttura si collegano tra loro come risultato della sovrapposizione di orbitali σ nell’ibrido sp³ di ciascuno di essi. Gli altri tre orbitali ibridati di ciascun atomo di carbonio si sovrappongono agli orbitali 1s degli atomi di idrogeno. Questo crea sei legami CH identici. Tali legami sono caratterizzati da un’energia di 420 kJ/mol. I legami CC hanno un’energia di 276 kJ/mol e una lunghezza di 1,54 Å.
Ibridazione sp²: Il Legame Doppio Carbonio-Carbonio
L'ibridazione sp² si ha quando un orbitale s si ibrida con 2 orbitali p. Si formano 3 orbitali ibridi isoenergetici. I 3 orbitali ibridi si dispongono sullo stesso piano con angoli di 120°, mentre l'orbitale p non ibridato si pone perpendicolarmente agli altri 3. Quando si sovrappone un orbitale p non ibridato di un C con quello di un altro C si ha un legame π, più debole del legame σ; quindi, tra due atomi di C si ha un doppio legame: uno σ e uno π.
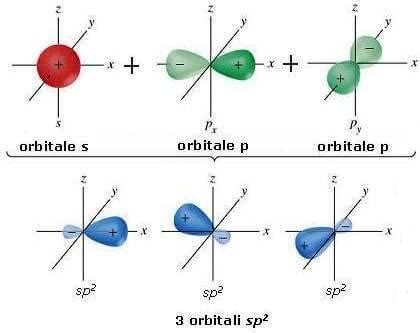
Nell’etilene (C₂H₄), come si può vedere dalla sua formula scritta sopra, due carbonii (C) sono legati fra loro da un doppio legame, e in più legano anche 2 idrogeni (H) ciascuno. In questo tipo di ibridazione, l’orbitale 2s del carbonio (C) si fonde con 2 sotto-orbitali di 2p formando 3 orbitali sp² che si dispongono a 120° l’uno dall’altro, in posizione TRIGONALE. L’ultimo sotto-orbitale p, rimasto vuoto, si dispone perpendicolarmente al piano formato dai 3 sp².
La ricerca ha rivelato che nell’etilene, ad esempio, gli atomi di carbonio mostrano una quantità adeguata di legami solo se si legano tra loro per condividere quattro elettroni. Quindi formano un doppio legame tra loro. Un altro fatto è che l’etilene ha una struttura piatta e gli angoli tra i suoi legami sono di 120 °. Questo perché in questo caso l’orbitale 2s si mescola con solo due dei tre orbitali 2p esistenti. Il risultato è la presenza di tre orbitali ibridati chiamati sp². Esiste anche un orbitale 2p, che non è ibridato. Come risultato della sovrapposizione degli orbitali sp²-sp², due atomi di carbonio con ibridazione sp² formano un legame σ. Gli orbitali p non ibridati degli atomi si sovrappongono lateralmente l’uno all’altro, il che provoca la formazione di un legame π. In un tale legame, le aree di densità elettronica sono presenti su entrambi i lati della linea tra i nuclei, anche se non direttamente tra di loro. Tale configurazione, che contiene un legame σ dell’ibrido sp² e un legame π di atomi non ibridati, porta a condividere quattro elettroni tra due atomi di carbonio, formando così un doppio legame C=C. Pertanto, la struttura dell’etilene contiene quattro atomi di idrogeno, che formano un legame σ con quattro orbitali sp² che rimangono una volta formato il doppio legame. La molecola ha una geometria piatta e gli angoli di legame sono di circa 120 °. I valori specifici del legame CH sono la lunghezza di 1.076Å e l’energia di 444 kJ/mol. Poiché sono condivisi solo due elettroni, non quattro (a differenza, ad esempio, della struttura dell’etano), il doppio legame C=C è più corto e più forte di un singolo legame CC. Nell’etilene ha una lunghezza di 1,33 Å e un’energia di 611 kJ/mol.
Con la teoria degli orbitali molecolari, possiamo anche osservare che la combinazione di due orbitali p atomici forma orbitali π molecolari di legame e antilegame. Un orbitale di legame non ha un nodo tra i nuclei a causa della combinazione additiva del p-loop con lo stesso segno algebrico. Al contrario, un orbitale antibonding ha un nodo tra i nuclei dovuto all’effetto sottrattivo del loop con diversi segni algebrici. Di conseguenza, viene riempito solo l’orbitale molecolare di legame meno energetico.
Ibridazione sp: Il Triplo Legame Carbonio-Carbonio
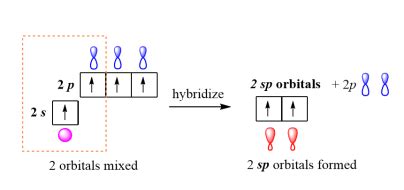
L'ibridazione sp si ha quando un orbitale s si sovrappone ad un solo orbitale p. I 2 orbitali ibridi ottenuti si dispongono lungo un asse con un angolo di 180°. Nei carboni coinvolti nel triplo legame, 1 orbitale s si fonde con 1 sotto-orbitale p formando 2 orbitali sp disposti a 180° l’uno dall’altro (disposizione DIGONALE).
Il triplo legame carbonio-carbonio costituisce il gruppo funzionale degli alchini. In un triplo legame ciascun atomo di carbonio è legato solo a due altri atomi e, in base alle regole di ibridazione, i legami σ verranno formati usando gli orbitali ibridi sp. Tali orbitali si legano secondo una linea retta che passa per il nucleo degli atomi di carbonio. Su ciascun atomo di carbonio di un triplo legame rimangono due orbitali atomici non ibridati 2p, disponibili per i legami π. Gli orbitali 2py di ciascun atomo possono sovrapporsi dando il legame π, che ha un lobo davanti e uno dietro rispetto all'asse della molecola. La coppia di orbitali adiacenti 2pz può combinarsi a sua volta per dare un secondo legame π i cui lobi siano sopra e sotto l'asse della molecola.
Scheletro dell'etino (acetilene, C₂H₂). La forza totale di legame (un legame σ + due orbitali π) è 196 Kcal/mole e la lunghezza di legame è 1,20 Å. Il triplo legame carbonio-carbonio è più forte e più corto del legame doppio.
Ibridazione orbitali sp, sp2, sp3
Un’altra possibilità di collegamento tra gli atomi di carbonio è la formazione di un triplo legame con sei elettroni condivisi. A questo scopo, dobbiamo introdurre un’altra ibridazione orbitale, chiamata ibridazione sp. In questa configurazione, l’orbitale 2s dell’atomo di carbonio si mescola solo con un singolo orbitale p. Ciò porta alla formazione di due orbitali con ibridazione sp e due orbitali p. Gli orbitali sp formano una struttura lineare e l’angolo tra loro è di 180 ° lungo l’asse x. Gli altri orbitali p sono perpendicolari agli altri assi (y e z). Quando due atomi di carbonio con ibridazione sp si sovrappongono, ciò provoca una sovrapposizione frontale che porta alla formazione di un forte legame σ (tipo sp-sp). Inoltre, si verifica la sovrapposizione laterale di entrambi gli orbitali p y - e p z , che forma legami π (tipo p y -p y ) e legami π (tipo p z -p z ) in quel particolare ordine. Di conseguenza, vengono condivisi sei elettroni, che formano un triplo legame C≡C. Gli orbitali sp formano una struttura lineare e l’angolo tra loro è di 180°. Gli altri orbitali p sono perpendicolari tra loro e all'asse degli orbitali sp.
Il triplo legame (rappresentato dal simbolo grafico ≡) è un tipo di legame covalente che si può instaurare tra due atomi in stato di ibridazione sp, formato da un forte legame σ e da due legami π più deboli a diversa energia, per un totale di sei elettroni di legame.
La molecola di acetilene, alchino di formula H-C≡C-H. In giallo sono evidenziati gli orbitali sp impegnati nei legami σ, mentre in blu e in viola sono evidenziati gli orbitali px e pz impegnati nei legami π. Lo stato di ibridazione di due atomi impegnati in un triplo legame prevede che ognuno dei due atomi possegga nel core elettronico esterno due orbitali ibridi sp (dati dalla combinazione di un orbitale s e di un orbitale p) e due orbitali p (indicati come px e pz), dove un orbitale sp ed i due orbitali p sono “fusi” a formare il triplo legame, mentre il restante orbitale sp è in genere impegnato a sua volta in un legame σ con l'orbitale ibrido di un altro atomo. Ne consegue che i due orbitali sp si trovano a 180° l'uno rispetto all'altro, essendo px e pz ortogonali tra di loro e tra gli orbitali ibridi. All'interno di una molecola organica un triplo legame definisce una struttura detta “lineare”.
A tale regola esistono tuttavia delle importanti eccezioni, primo tra tutti il caso particolare dei cicloalchini, famiglia di molecole organiche in cui il triplo legame è incluso in una struttura ciclica e dove quindi il gruppo R-C≡C-R', per motivi geometrici, non può essere lineare. Una delle eccezioni riguardo alla geometria lineare del triplo legame si ha con l'instaurarsi di un legame dove almeno uno dei due atomi è in grado di espandere l'ottetto. È questo ad esempio il caso del trifluoruro di tiazile, composto inorganico di formula F₃S≡N dove l'atomo di zolfo è impegnato in quattro legami, tre dei quali singoli ed uno triplo. La geometria di legame, in questo specifico caso, è tetraedrica. Non necessariamente, tuttavia, un triplo legame che coinvolge un atomo in grado di espandere l'ottetto esulerà dalla regola generale della geometria lineare.
La reattività del triplo legame è determinata dalla natura dei due atomi, uguali o diversi, legati tra di loro. In genere i composti organici sono soggetti a reazioni di riduzione o di addizione sul triplo legame, che vedono lo spezzarsi di uno o di entrambi i legami π e la consecutiva ibridazione degli orbitali px e pz a sp. Anche i composti inorganici contenenti legami tripli sono molto reattivi, come nel caso del monossido di carbonio (gas tossico instabile in presenza di ossigeno), del monosolfuro di carbonio (con tendenza a polimerizzare) e dello ione cianuro (tossico per formazione di complessi stabili con proteine deputate alla respirazione cellulare).
Alcune molecole organiche soggette al fenomeno della risonanza possono presentare forme limite che contengono legami tripli. Da notare che in entrambe le forme limite il carbonio ha ibridazione sp, mentre l'ossigeno ha ibridazione sp³ nella prima forma e sp² nella seconda e l'azoto sp nella prima e sp² nella seconda. Più complessa è invece la risonanza di composti come i sali di diazonio arilici, di formula Ar-N≡N⁺. Nella prima forma, i carboni dell'anello aromatico sono tutti in stato di ibridazione sp², mentre i due atomi di azoto hanno ibridazione sp. Nelle successive forme limite l'azoto direttamente legato all'anello mantiene ibridazione sp, mentre il secondo azoto ha ibridazione sp².
Argomenti Correlati: Energia di Legame e Carattere Sull'Orbitale Ibrido
Il legame C-H in una ibridizzazione sp è più forte di quello sp³ per il fatto che è contraddistinto da un legame sigma e due pi-greco. Questo significa che avendo tre legami con un solo atomo di idrogeno, gli orbitali del carbonio e dell'idrogeno sono più vicini tra loro rispetto alla configurazione sp³ in cui essi avendo un solo legame sigma sono più distanti, e dunque posseggono minore energia di legame. Un legame sigma è un legame che passa tra i due atomi coinvolti "da nucleo a nucleo", mentre il legame pi-greco risiede "sopra e sotto" i nuclei degli atomi coinvolti nel legame. Inoltre un orbitale sp è costituito dal 50% di orbitale s e dal 50% di orbitale p. L'orbitale s è rappresentato come una sfera; cosa sono i nodi? Sono regioni di spazio orbitalico in cui la probabilità di trovare l'elettrone è molto bassa, se non nulla. L'orbitale s è piuttosto grande rispetto a quello p quindi se vi è una maggiore presenza di s rispetto a p ecco spiegata la maggiore energia di legame. In un orbitale sp³ la percentuale di carattere s è solo del 25% mentre quella dell'orbitale p del 75% (correzione rispetto al testo originale che indica 23% e 77% per sp3, il calcolo corretto per sp3 è 1/4=25% s e 3/4=75% p, mentre per sp2 è 1/3 s e 2/3 p, e per sp è 1/2 s e 1/2 p). L'orbitale p è più piccolo di quello s ed inoltre è disposto su tutti e tre gli assi dello spazio tridimensionale x,y,z. Minore è la percentuale di carattere s nell'orbitale ibrido minore è l'energia di legame.
La forza di un legame dipende da quanto la sovrapposizione orbitalica è efficace ma anche dalla distanza dai nuclei degli orbitali che si sovrappongono. Se ora mi immagino due orbitali ibridi: uno con più carattere "s" (sp) e l'altro "p" (sp³) per capire quale si sovrappone meglio con l'orbitale "s" di un H dovrei quindi fare due ragionamenti: a) uno sulla distanza a cui avviene la sovrapposizione b) uno sull'entità (efficacia) della sovrapposizione in funzione della simmetria degli orbitali. Per il primo punto, a), è evidente che essendo i due orbitali ibridi sp² ed sp³ ottenuti entrambi con un "mescolamento" di orbitali atomici tutti appartenenti a uno stesso livello "n" (rispettivamente 1s, 2p e 1s, 3p) avranno entrambi una distanza più o meno uguale dal nucleo. È un'operazione matematica che comporta la formazione di orbitali elettronici misti mediante una combinazione lineare di funzioni d'onda appropriate. Il lavoro su questo tema risale al 1931, quando Linus Pauling suggerì la risposta alla struttura del metano - come disposizione spaziale dei legami. Il composto organico più semplice è la molecola di metano, che contiene un atomo di carbonio. Il suo guscio di valenza ha quattro elettroni, quindi è in grado di produrre quattro legami, e in una molecola di metano - con quattro atomi di idrogeno. Inizialmente si presumeva che a causa dell’uso di due tipi di orbitali (2s e 2p) durante la formazione dei legami, il metano avesse due diversi tipi di legami CH. Tuttavia, ulteriori ricerche hanno rivelato un’altissima probabilità che, nonostante questi presupposti, ogni legame CH esistente nel metano sia identico e spazialmente diretto verso gli angoli di un tetraedro regolare. È stato Linus Pauling a rispondere alla domanda perché è così. Ha dimostrato matematicamente come sia possibile l’ibridazione, cioè la miscelazione di un orbitale s con tre orbitali p. Ciò provoca la formazione di quattro orbitali atomici equivalenti la cui geometria spaziale ha la forma del tetraedro. Questo tipo di ibridazione è chiamato sp³.
Il legame CH nell’acetilene (etino) ha la lunghezza di 1.06Å e l’energia di 552 kJ/mol. La lunghezza di quel legame è minore e la sua energia è maggiore rispetto ai legami singoli e doppi. Questi valori sono rispettivamente 1,20Å (per il legame C-C singolo) e 835 kJ/mol (per il legame C≡C triplo).
Applicazioni Generali dell'Ibridazione
I concetti di tre tipi di ibridazione (sp, sp² e sp³) sono applicabili non solo in strutture che contengono atomi di carbonio. La molecola dell’ammoniaca (NH₃) - l’atomo di azoto ha cinque elettroni di valenza e produce tre legami atomici, che si avvicinano a un ottetto. L’angolo di legame HNH è stato misurato sperimentalmente; è uguale a 107,3 °, quindi è vicino all’angolo tetraedrico. Ciò suggerisce che l’ammoniaca dovrebbe essere considerata nel contesto di sp³. L’atomo di azoto si ibrida con la formazione di quattro orbitali sp³; uno di essi ha due elettroni di non legame, mentre ogni altro orbitale contiene un elettrone di legame.
La molecola dell’acqua (H₂O) - l’atomo di ossigeno mostra anche sp³. Tuttavia, contiene sei elettroni di valenza, quindi forma due legami atomici, lasciando due coppie di elettroni libere. L’angolo di legame HOH nella molecola è 104,5 °, quindi è anche simile all’angolo tetraedrico, il che suggerisce l’ibridazione. Qualsiasi valore di quell’angolo inferiore è probabilmente il risultato di ben due coppie di elettroni libere, che si allontanano a vicenda.
La molecola del fluoruro di boro (BF₃) - l’atomo di boro include tre elettroni di valenza, quindi può produrre solo tre legami senza raggiungere un ottetto. Tuttavia, gli atomi esistenti di fluoro formano legami BF con esso, disposti spazialmente il più lontano possibile l’uno dall’altro.
In particolare, l'esercizio 1 fornito nel materiale di origine chiede: Quanti e quali legami ha la molecola C₃H₄? La formula della molecola scritta in forma distesa è la seguente: CH₃-C≡CH. Il carbonio 1 è quello sulla destra in quanto si incomincia a numerare dal carbonio più vicino al triplo legame. C1 forma un legame σ con l’H, C3 forma 3 legami σ con i 3 H e un altro legame σ con C2. C1 e C2 hanno un triplo legame che li lega, di questi uno è un legame σ e gli altri due sono π. Analizzando la struttura CH₃-C≡CH, abbiamo:
- Il carbonio terminale del CH₃ è ibridato sp³ e lega 3 H con legami σ e un altro C con un legame σ.
- Il carbonio centrale del triplo legame è ibridato sp e lega un altro C con un legame σ e due legami π.
- Il carbonio terminale del triplo legame è ibridato sp e lega un H con un legame σ e un altro C con un legame σ e due legami π.Quindi, contando i legami σ: 3 (C-H) + 1 (C-C sp³-sp) + 1 (C-C sp-sp σ) + 1 (C-H sp-H) = 6 legami σ. Ci sono poi 2 legami π nel triplo legame C≡C. La risposta corretta è quindi 6 legami σ e 2 legami π (opzione C).
tags: #triplo #legame #ibridazione