Il carbonio, elemento simbolo C, si erge come una pietra miliare nella chimica, tessendo le trame della vita e costituendo la spina dorsale della chimica organica e delle macromolecole biologiche essenziali come proteine e acidi nucleici. Nei mammiferi, ad esempio, rappresenta circa il 22% del peso corporeo, testimoniando la sua ubiquità e importanza. Appartenente al IV gruppo della tavola periodica, questo non metallo possiede un peso atomico di 6 e una massa atomica di 12. La sua abbondanza naturale è dominata dall'isotopo 12, che costituisce circa il 98,8%, seguito dall'isotopo 13 con circa l'1%. L'isotopo 14, presente in tracce, riveste un'importanza storica fondamentale grazie al suo impiego nella datazione di reperti archeologici.
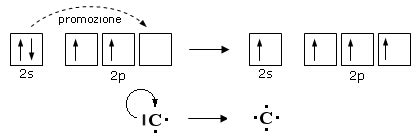
La configurazione elettronica del carbonio, 1s²2s²2p², rivela un livello energetico esterno con un orbitale di tipo s e tre orbitali di tipo p. In questo stato, l'orbitale s contiene due elettroni appaiati, due orbitali p ospitano ciascuno un elettrone spaiato, mentre l'ultimo orbitale p rimane vuoto. Questa disposizione consente al carbonio di formare fino a quattro legami covalenti, corrispondenti al riempimento completo dei suoi orbitali. Tuttavia, la versatilità del carbonio emerge con prepotenza attraverso il fenomeno dell'ibridazione, dove gli orbitali s e p si fondono per creare nuovi orbitali ibridi con geometrie e orientamenti specifici, permettendo la formazione di legami con caratteristiche uniche.
L'Ibridazione sp3: La Genesi della Struttura Diamantina
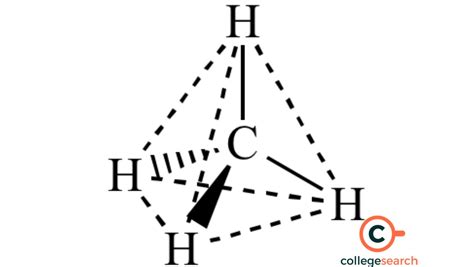
Tra le diverse forme di ibridazione che il carbonio può adottare, l'ibridazione sp3 riveste un'importanza cruciale per la formazione di strutture cristalline eccezionalmente stabili e dure, come il diamante. Questo processo deriva dalla fusione di un orbitale s con tre orbitali p, dando origine a quattro orbitali ibridi identici. Questi orbitali si dispongono nello spazio secondo una geometria tetraedrica, con un angolo di 109,5° tra ciascuna coppia di orbitali. Ogni orbitale ibrido sp3 è orientato verso i vertici di un tetraedro equilatero, pronto a formare legami covalenti.
Nel contesto dell'ibridazione sp3, ogni orbitale ibrido può formare un legame sigma (σ) con un altro orbitale, sia esso un altro orbitale ibrido di un atomo di carbonio adiacente o un orbitale di un altro elemento. Il legame sigma è caratterizzato dalla sovrapposizione frontale degli orbitali, che crea una densità elettronica lungo l'asse internucleare, conferendo una notevole forza e stabilità al legame.
Il Diamante: Un Reticolo Cristallino di Eccezionale Durezza
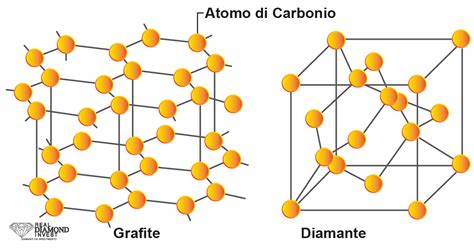
Il diamante, una delle forme allotropiche più note del carbonio, è l'incarnazione dell'ibridazione sp3. In questa struttura cristallina, ogni atomo di carbonio è saldamente legato ad altri quattro atomi di carbonio, ciascuno posizionato ai vertici di un tetraedro. Questa disposizione crea un reticolo tridimensionale estremamente ordinato e coeso, dove i legami covalenti si estendono in tutte le direzioni.
La struttura chimica del diamante è direttamente responsabile delle sue straordinarie proprietà fisiche, in particolare della sua durezza eccezionale. Secondo la scala di Mohs, che classifica la resistenza dei minerali alla scalfittura, il diamante occupa il gradino più alto (10), essendo considerato il materiale più duro in natura. Questa durezza, tuttavia, può essere influenzata dalla presenza di impurezze nel reticolo cristallino.
La natura del legame covalente puro nel diamante, esteso a tutta la struttura, conferisce una stabilità eccezionale. A differenza di molti solidi cristallini in cui si possono identificare molecole discrete con coesione relativamente debole tra di esse, il diamante può essere considerato una macromolecola unica. Non esistono molecole discrete nel reticolo diamantino; l'intero cristallo è interconnesso da un'estesa rete di legami covalenti sp3.
I cristalli di diamante grezzo, formatisi a grandi profondità sotto immense pressioni e temperature, spesso presentano deformazioni, spigoli e vertici arrotondati. Questo è il risultato dell'erosione superficiale subita durante il loro trasporto verso la crosta terrestre, avvenuto attraverso i cosiddetti "camini diamantiferi".
Il concetto di durezza in un corpo solido si riferisce alla resistenza che esso oppone alla scalfittura, all'abrasione o alla penetrazione. Questa proprietà è intrinsecamente legata al grado di coesione all'interno del reticolo cristallino, determinato dalla varietà di combinazioni di legami. La scala di Mohs, sebbene ampiamente utilizzata, si basa su criteri empirici e sulla sensazione tattile, con intervalli non matematicamente uniformi tra i valori. Per una misurazione più quantitativa della resistenza all'abrasione, si utilizza la scala di Rosiwal.
Il diamante esibisce anisotropia per quanto riguarda la durezza, mostrando una resistenza maggiore lungo certe direzioni cristallografiche rispetto ad altre. La sua struttura cristallina compatta, con atomi di carbonio legati in una disposizione tetraedrica distanziati di circa 1,54 Å l'uno dall'altro, lo rende poco elastico e, di conseguenza, fragile. Questa fragilità richiede particolare attenzione durante le operazioni di taglio e incastonatura, dove il rischio di frattura o scheggiatura è significativo. La facile sfaldatura lungo i piani dell'ottaedro è una proprietà sfruttata per la lavorazione del diamante grezzo.
Dal punto di vista cristallografico, il diamante appartiene al sistema monometrico (o cubico), con un habitus cristallino che può essere ottaedrico o esacistoedrico, caratterizzato da un elevato grado di simmetria. Dal punto di vista ottico, è un minerale monorifrangente, il che significa che la velocità della luce è la stessa in tutte le direzioni, rendendolo isotropo. Tuttavia, irregolarità nel reticolo cristallino, dovute a tensioni durante la cristallizzazione o alla presenza di impurità, possono indurre una birifrangenza anomala.
Sottoposto a radiazioni ultraviolette, il diamante può manifestare fluorescenza, con colori che variano dal blu al giallo, verde e rosa, il blu essendo il più comune. Questa caratteristica è un importante elemento distintivo per i laboratori di analisi gemmologica e influisce sulla valutazione commerciale della gemma.
INCREDIBILE Come si Fanno i DIAMANTI nella Terra💎
Proprietà Anomale: Conducibilità Termica ed Elettrica
Un aspetto particolarmente interessante del diamante è il suo comportamento anomalo riguardo alla conducibilità termica ed elettrica. Possiede un'elevatissima conducibilità termica, compresa tra 1000 e 2600 W/m·K, una proprietà che lo rende un eccellente conduttore di calore. Questa caratteristica è sfruttata in applicazioni microelettroniche per la dissipazione efficiente del calore.
Al contrario, il diamante è un eccellente isolante elettrico. Gli elettroni di valenza del carbonio sono completamente impegnati nei legami covalenti sp3, rendendoli non liberi di muoversi e di condurre corrente elettrica. Questo contrasta nettamente con la grafite, un'altra forma allotropica del carbonio, dove gli elettroni sono delocalizzati e contribuiscono a una buona conducibilità elettrica. Nel diamante, l'energia termica viene trasmessa non dagli elettroni, ma dalle vibrazioni del reticolo cristallino, un fenomeno noto come fononi. La rigidità del reticolo e la bassa massa degli atomi di carbonio contribuiscono all'elevata conducibilità termica.
La Formazione del Diamante: Condizioni Estreme di Pressione e Temperatura
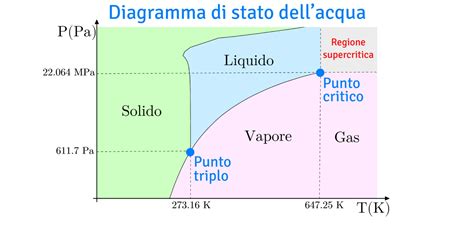
La formazione del diamante è un processo che richiede condizioni estreme di pressione e temperatura. Studi di laboratorio indicano che il diamante cristallizza a pressioni di almeno 50 kbar e temperature superiori a 900 °C. Al di sopra dei 1200 °C, in queste condizioni di pressione, tende a riformarsi la grafite. Pertanto, il campo di stabilità del diamante si situa tra i 900 °C e i 1200 °C a pressioni di circa 50 kbar.
Queste condizioni si ritrovano tipicamente nelle profondità della Terra, in particolare nei vecchi cratoni stabili che costituiscono il nucleo dei continenti antichi. Questi cratoni, formatisi oltre 2,5 miliardi di anni fa, hanno subito pochi eventi tettonici significativi, mantenendo condizioni di temperatura relativamente moderate a grandi profondità.
Durante il trasporto verso la superficie, il diamante attraversa zone con condizioni di temperatura e pressione diverse da quelle del suo campo di stabilità. Per evitare la trasformazione in grafite o la combustione, il trasporto deve avvenire in modo estremamente rapido. Questo avviene attraverso l'ascesa di magmi, noti come kimberliti, a velocità valutate tra i 40 e i 70 km/h. La durata di questo processo di trasporto è ancora oggetto di dibattito, con stime che vanno da 900 milioni a tre miliardi di anni.
La litogenesi del diamante è di tipo magmatico intrusivo. Quando un magma, per varie ragioni, si raffredda al di sotto della sua temperatura di fusione in profondità, tende a cristallizzare.
Oltre il Diamante: La Diversità Allotropica del Carbonio
Il carbonio, nella sua intrinseca versatilità, manifesta una ricca gamma di forme allotropiche, ognuna con proprietà uniche derivanti dalle diverse modalità di legame e organizzazione atomica. Oltre al diamante, il carbonio puro si presenta in altre forme straordinariamente diverse:
Grafite: Caratterizzata da ibridazione sp2, la grafite forma strutture esagonali disposte su piani paralleli. Ogni atomo di carbonio è legato ad altri tre atomi di carbonio, mentre un elettrone p non ibridato per atomo forma legami pi greco (π) perpendicolari al piano del reticolo. Questi legami π conferiscono alla grafite la sua buona conducibilità elettrica. I piani sono tenuti insieme da deboli interazioni di Van der Waals, rendendo la grafite morbida e scivolosa.
Fullereni: Scoperti più recentemente, i fullereni sono molecole di carbonio con strutture sferiche o ellissoidali. Il buckminsterfullerene (C60), con la sua forma simile a un pallone da calcio composta da 20 esagoni e 12 pentagoni, è il più noto. I fullereni sono stabili a temperatura e pressione ambiente e poco reattivi. Studi in campo biomedico esplorano il loro potenziale come agenti terapeutici, ad esempio per combattere la resistenza agli antibiotici o per indurre la morte selettiva di cellule cancerose.
Nanotubi di Carbonio: Si formano quando fogli di grafene si arrotolano su sé stessi, creando strutture cilindriche. Possono essere a parete singola o multipla. I nanotubi di carbonio sono noti per la loro eccezionale resistenza meccanica e possono agire come conduttori elettrici, semiconduttori o isolanti a seconda del loro diametro. Le loro applicazioni spaziano dalla meccanica alla medicina, con particolare interesse per lo sviluppo di biosensori chimici e biologici.
Grafene: Un singolo strato di atomi di carbonio disposti in un reticolo esagonale. Il grafene è un materiale bidimensionale con proprietà elettriche, meccaniche e termiche eccezionali, aprendo la strada a nuove tecnologie in elettronica, materiali compositi e immagazzinamento di energia.
Carbonio Simile al Diamante (DLC): Si tratta di un materiale amorfo metastabile le cui proprietà meccaniche, elettriche, ottiche e tribologiche sono simili a quelle del diamante. Il DLC presenta un'elevata conducibilità termica, buona stabilità chimica e eccellente inerzia chimica. La definizione standard internazionale per la durezza di un film DLC è basata sulla durezza del diamante naturale.
Pentadiamond: Un nuovo materiale a base di carbonio, progettato per sostituire i diamanti sintetici nelle applicazioni industriali di taglio e perforazione. La sua configurazione atomica e la densità elettronica sono studiate attraverso metodi computazionali avanzati come la teoria funzionale della densità (DFT).
Queste diverse forme allotropiche del carbonio, originate dalla capacità dell'elemento di formare una varietà di stati ibridi, evidenziano la straordinaria versatilità di questo elemento fondamentale. L'ibridazione sp3, in particolare, è la chiave della struttura compatta e della durezza senza pari del diamante, un materiale che continua ad affascinare scienziati e ingegneri per le sue proprietà uniche e le sue molteplici applicazioni.
La comprensione approfondita delle diverse forme di ibridazione del carbonio, dall'sp3 all'sp2 e all'sp, è essenziale per decifrare le proprietà di un'ampia gamma di materiali, dai composti organici più semplici alle strutture nanotecnologiche più avanzate. La capacità del carbonio di adattarsi a differenti geometrie di legame è alla base della sua centralità in chimica e scienza dei materiali.
tags: #carbonio #ibridazione #sp3 #diamante